

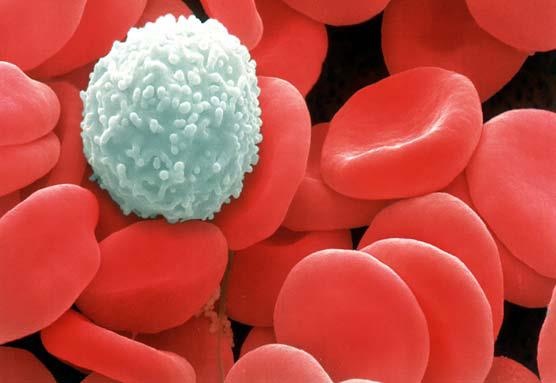
Mutaties die zich voordoen in de voorlopers van de bloedcellen kunnen leiden tot de productie van een overdaad aan onrijpe cellen en tot bloedkanker. Wij analyseren de mechanismen die aanleiding geven tot dergelijke mutaties. We bekijken nieuwe therapeutische benaderingen door receptoren van groeifactoren of van activatoren (JAK genoemd) af te remmen en door weerstand tegen chemotherapie te bestuderen.
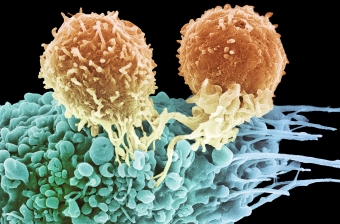
Ons afweersysteem is in staat om kankercellen van normale cellen te onderscheiden en selectief te doden. We bestuderen de mechanismen die in dit proces betrokken zijn. Het doel is immuuntherapie te ontwikkelen, een therapeutische aanpak waarbij afweerreacties tegen tumoren gestimuleerd worden.
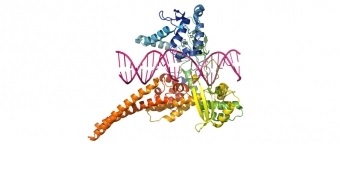
Kanker wordt veroorzaakt door DNA mutaties, die vaak een invloed hebben op interne cel signalering. Wij zijn vooral geïnteresseerd in enzymen genoemd "tyrosine kinases" en kleine remmende RNA, die de ontwikkeling van tumoren controleren. Deze spelen een belangrijke rol in kanker diagnose en therapie.
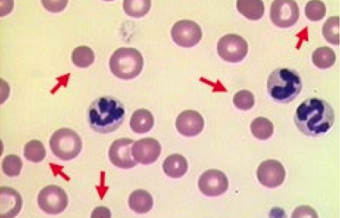
Cellen staan bloot aan aanzienlijke veranderingen in hun vorm, zoals het geval is voor rode bloedcellen die door zeer smalle bloedvaten stromen. Verminderde weerstand tegen celwandvervormingen veroorzaakt "fragiele membraan ziektes". We bestuderen de organisatie van membraanlipiden en hun rol in de vervorming van celmembranen, om een beter begrip te krijgen van deze ziektes en de ontwikkeling ervan te kunnen voorkomen.
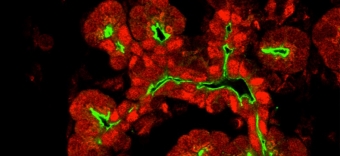
De functie en vorm van de organen worden bepaald tijdens de embryonale ontwikkeling. Wij onderzoeken hoe de lever, alvleesklier en schildklier zich ontwikkelen in embryos, en hoe abnormale reactivatie van embryonale processen in adulte weefsels kan leiden to ziektes. Wij onderzoeken ook hoe stamcellen de integriteit van de huid en nieren handhaven, in normale situaties en in pathologieën.

We bestuderen de genetische variaties die aan de basis liggen van ziekten bij de mens. We concentreren ons op vasculaire anomalieën, lymfoedeem, gespleten lip en verhemelte, hypermobiliteit en een selectie van kankers. We identificeren DNA-mutaties die deze ziekten in de hand werken of veroorzaken om de moleculaire mechanismen ervan te begrijpen en om doelwitten te identificeren voor de ontwikkeling van nieuwe therapieën.
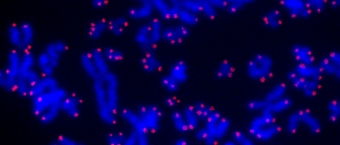
Genetische informatie wordt behouden in ons DNA , en mutaties die de struktuur van DNA aantasten kunnen kanker veroorzaken. Wij bestuderen hoe kanker kan ontstaan ten gevolge van epigenetische veranderingen, d.w.z veranderingen die de functie maar niet de struktuur van DNA wijzigen. Telomeren zijn DNA fragmenten aan de uiteinde van chromosomen die de onsterfelijkheid van kankercellen vrijwaren. Wij onderzoeken ook hoe kankercellen de integriteit van telomeren handhaven.
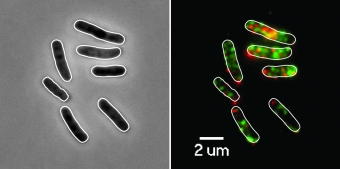
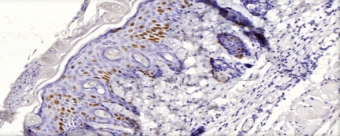
Virussen werken als parasieten van de cellen en dus zijn ze vaak schadelijk voor hun gastheer en veroorzaken ziekten. Ze zijn echter ook afhankelijk van gastheercellen om zich te vermenigvuldigen en zijn daarom zo geëvolueerd dat hun gastheer behouden blijft. Onze teams onderzoeken de interactie van virussen met hun gastheercellen, die werken als immuuncellen die de infectie bestrijden of als gastheercellen die het doelwit zijn van een virusinfectie.
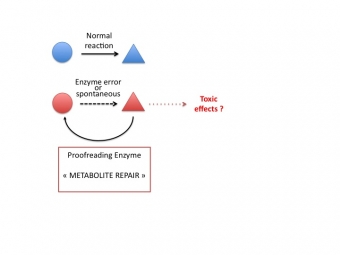
Ons werk is gericht op de opheldering van ‘aangeboren fouten in het metabolisme’, van ziekten die te wijten zijn aan een erfelijk enzymatisch gebrek. Een van ons doelstellingen is het gen dat codeert voor verschillende enzymen waarvoor deze informatie ontbreekt te identificeren. Een andere doelstelling bestaat erin nieuwe enzymen te ontdekken, vooral dan enzymen die een rol spelen in het herstel van het metabolisme.
Weefsels die ons lichaam samenstellen zijn dynamische structuren. Een opmerkelijk voorbeeld hiervan is het endometrium (de baarmoeder slijmvlies) die een cyclische afbraak ondergaat (menstruatie), gevolgd door een regeneratie zonder litteken. Wij zijn geïnteresseerd in de mechanismen van deze weefselremodellering en hun pathologische afwijkingen (abnormale baarmoeder bloeden en endometriose).
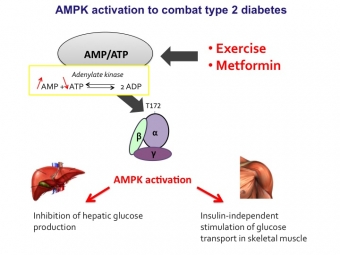
Diabetes van het type 2 kan in eerste instantie worden beheerd met regelmatige lichaamsbeweging, welke AMPK activeert, en in een later stadium pas door behandeling met geneesmiddelen. We testen kleine moleculen voor hun mogelijke activering van AMPK, vooral in spier en lever, om de glucosespiegel in het bloed te verlagen en zo de ziekte te bestrijden. We proberen ook om, met behulp van state-of-the-art massaspectrometrische methoden, nieuwe AMPK targets te identificeren.

Modern high throughput biology produces huge amounts of data that can be analyzed, and the challenges of modern biology are statistical interpretation and integration of these data. Research and developments in computational biology and bioinformatics aim to provide the methods and tools to comprehend these high dimensional data and understand their underlying biological processes.