

(d'après ScienceToday)
06/05/2020
| La Pre Maria Veiga-da-Cunha a reçu le prix Alvarenga de Piauhy de l'Académie royale de médecine de Belgique pour cette success story |
Une découverte en recherche fondamentale débouche sur le traitement de maladies rares affectant le système immunitaire. De nombreux patients atteints de ces maladies sont actuellement traités dans le monde sur base de cette success story réalisée par les chercheurs de l’Institut de Duve à l’UCLouvain.
Les neutrophiles sont des globules blancs qui jouent un rôle majeur dans notre système immunitaire. Ils sont en première ligne pour combattre les bactéries qui infectent notre organisme. Mais certaines maladies entraînent une baisse de la quantité de neutrophiles présents dans le sang, on parle de ‘neutropénie’. Ceci a pour conséquence que les patients atteints de ces maladies font plus facilement des infections graves. C’est le cas d’une maladie métabolique appelée glycogénose de type Ib. Ce n’est que tout récemment que la cause de la neutropénie dans cette maladie, mais également dans une deuxième maladie rare apparentée, a été comprise par l’équipe dirigée par les professeurs Maria Veiga-da-Cunha et Emile Van Schaftingen à l’Institut de Duve de l’UCLouvain et publiée en 2019 dans la revue PNAS (plus d'informations dans ScienceToday).
| Le témoignage d'un patient qui a vu sa vie transformée par cette découverte |
Ces chercheurs ont montré que les neutrophiles de ces malades sont intoxiqués par un dérivé phosphorylé d’une molécule ressemblant au glucose (le 1-désoxyglucose) que nous avons tous dans le sang. Le défaut génétique présent chez les patients atteints de cette maladie fait que le dérivé phosphorylé du 1-désoxyglucose s’accumule et perturbe profondément le métabolisme des neutrophiles. Sur base de cette découverte, ces chercheurs ont proposé de traiter cette maladie avec un médicament antidiabétique qui abaisse la concentration de glucose dans le sang en augmentant son élimination dans les urines. Ce médicament provoque aussi l’élimination du 1-désoxyglucose et entraîne donc un abaissement de sa concentration dans le sang. Logiquement, les chercheurs ont pensé que ce médicament devait donc également diminuer l’accumulation du dérivé toxique du 1-désoxyglucose dans les neutrophiles. Leurs expériences faites sur souris ont montré que c’était bien le cas.
Dans un article qui vient de paraître dans la revue Blood, l’équipe de l’UCLouvain, en collaboration avec des cliniciens d’Autriche, des Etats-Unis et des Pays-Bas, montre que ce traitement révolutionnaire fonctionne chez les patients. Ceux-ci (quatre au total) présentaient des infections récurrentes de la bouche, de l’intestin et/ou de la peau, avec impossibilité pour certains d’entre eux d’arriver à se nourrir normalement, avec des diarrhées persistantes et/ou des plaies surinfectées qui ne cicatrisaient pas. L’administration de l’antidiabétique a fait disparaître, ou pratiquement disparaître, ces symptômes en quelques semaines. Le nombre de neutrophiles dans le sang s’est stabilisé et surtout, les neutrophiles ont récupéré leur capacité de s’attaquer efficacement aux bactéries.
|
|
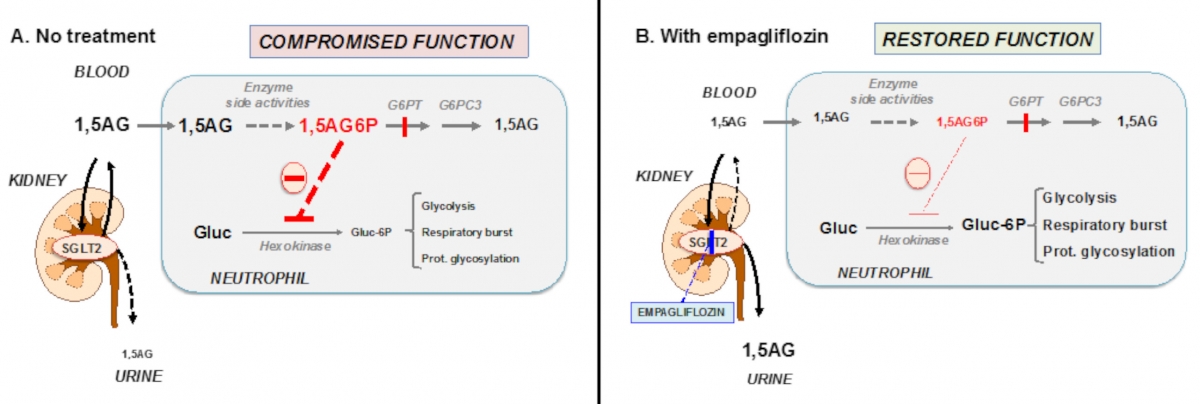
L’antidiabétique empagliflozine fait chuter le taux plasmatique de 1,5-anhydroglucitol et restaure la fonction des neutrophiles chez les patients atteints de GSD-Ib en abaissant le taux de 1,5-anhydroglucitol-6-phosphate des neutrophiles. Le 1,5-anhydroglucitol (1,5-AG) est un analogue du glucose non métabolisable présent dans le sang (≈150 µM) qui provient de l'alimentation. Il est lentement phosphorylé en 1,5-anhydroglucitol-6-phosphate (1,5-AG6P) par des activités secondaires des hexokinases et de la glucokinase dépendante de l'ADP (ADPGK) présentes dans les neutrophiles. Pour empêcher son accumulation, qui bloque la phosphorylation du glucose (voir ci-dessous), le 1,5AG6P est transporté dans le réticulum endoplasmique par un transporteur appelé G6PT, et déphosphorylé par la phosphatase G6PC3. Panneau A : chez les patients GSD-Ib, déficients en G6PT, le 1,5AG6P s'accumule dans les neutrophiles. C'est l'augmentation de la concentration de 1,5AG6P qui intoxique les neutrophiles en inhibant fortement les hexokinases et en épuisant le pool intracellulaire de glucose-6-phosphate (Gluc-6P) qui est vital pour la survie et le fonctionnement des neutrophiles. Panneau B : L'inhibition par l’empagliflozine du transporteur (SGLT2) permettant la réabsorption du glucose dans le tube dans le rein conduit à une glucosurie, ainsi qu’à une élimination urinaire accrue du 1,5-AG. Ceci à pour conséquence de réduire d’environ 4 fois tant la concentration de 1,5-AG dans le sang et que celle du 1,5-AG6P dans les neutrophiles. Les hexokinases ne sont plus inhibées, ce qui augmente le pool de glucose-6P et des métabolites se situant en aval, améliorant ainsi la glycolyse, le « respiratory burst » et la glycosylation des protéines. Les neutrophiles fonctionnent mieux et la neutropénie est en grande partie corrigée. |
De nombreux autres patients atteints des deux neutropénies rares apparentées sont actuellement traités dans le monde sur base des découvertes faites par l’équipe de l’Institut de Duve. Les recherches menant à ces découvertes ont été soutenues financièrement par diverses sources de financement (le FNRS, UCLouvain, l’Institut de Duve), et tout particulièrement par WELBIO. “Cette étude marque une étape clef pour WELBIO”, souligne Pierre Van Renterghem, Directeur Général de WELBIO, l’institut wallon de recherche d’excellence dans les domaines des sciences de la vie. “Des patients bénéficient aujourd’hui d’un traitement qui n’a pu être imaginé que grâce à des découvertes fondamentales concernant le métabolisme intermédiaire, effectuées dans le cadre d’un projet de recherche soutenu par WELBIO. Moins de 10 ans après le démarrage de nos activités, il s’agit du premier de nos projets où les chercheurs passent avec succès de la recherche fondamentale au traitement de patients“

|
|
Emile Van Schaftingen and Maria Veiga-da-Cunha |
Article décrivant ces recherches
Wortmann SB, Van Hove JLK, Derks TGJ, Chevalier N, Knight V, Koller A, Oussuren E, Mayr JAM, van Spronse FJ, Lagler FB, Gaughan S, Van Schaftingen E, Veiga-da-Cunha M
Blood (2020)
La presse en parle
L'avenir.net - Grâce à des chercheurs belges, on a un traitement pour une maladie rare - 05/05/2020
Journal of Inherited Metabolic Disease (JIMD Editorial) - View from inside: Nina, Glycogen storage disease warrior - 07/05/2020
Biovox - Fundamental research leads to treatment breakthrough in rare genetic diseases - 08/06/2020
 |
|
View from inside: Nina, Glycogen storage disease warrior Du diagnosis au traitement: le témoignage poignant des parents de Nina, atteinte de glycogénose de type 1b, une maladie métabolique héréditaire. Retrouvez comment les découvertes de Maria Veiga da Cunha, Emile Van Schaftingen, Guido Bommer et de leurs collaborateurs internationaux ont redonné de l'espoir à Nina. |
|
How empagliflozin helps treat neutropenia in glycogen storage disease type 1b ? De la recherche fondamentale au traitement : regardez comment la découverte de Maria Veiga da Cunha, Emile Van Schaftingen et Guido Bommer (investigateurs Welbio) et leurs collaborateurs internationaux donne de l'espoir aux patients souffrant de glycogénose de type 1b, une maladie métabolique héréditaire. |