

26/04/2019
Leverkanker, meer specifiek hepatocellulair carcinoom (HCC) - een tumor die in hepatocyten wordt geïnitieerd - is wereldwijd de op twee na meest voorkomende doodsoorzaak bij kanker. De ziekte kan het gevolg zijn van verschillende aandoeningen zoals virale infecties of cirrose en dat leidt tot een significante heterogeniteit bij patiënten en een variabele respons op therapeutische middelen. Daarom is er behoefte aan het ontwikkelen van therapieën die specifiek zijn voor individuele patiënten.
De ziekte is geassocieerd met de gelijktijdige deregulering van verschillende genen die functioneel georganiseerd zijn als netwerken. Het is het netwerk als geheel, niet een individueel gen, dat de voortgang van de kanker beïnvloedt. Hoe een specifiek netwerk wordt beïnvloed verschilt van patiënt tot patient. Daarom zouden we tools moeten hebben die het gedrag van gennetwerken in individuele patiënten kunnen voorspellen.
In deze studie identificeerden Claude Gérard, Mickael Di-Luoffo, Léolo Gonay en Frédéric Lemaigre een functioneel gennetwerk dat betrokken is bij HCC en gastro-intestinale kankers (zie onderstaande figuur). De netwerkstatus correleert negatief met de vitale prognose bij HCC en correleert positief met hyperproliferatie van de tumorcellen.
 |
|
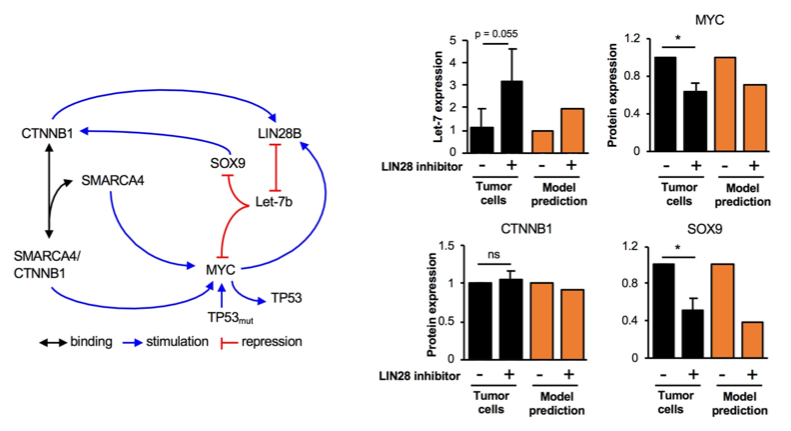
Gennetwerk dat de groei van een hepatocellulair carcinoom aandrijft. Links: structuur van het netwerk. CTNNB1 (beta-catenine), MYC, LIN28 zijn oncogenen in HCC, TP53 en Let-7 zijn tumorsuppressoren. Rechts: effect van een op LIN28 gericht medicijn op andere genen van het netwerk, zoals gemeten in primaire tumorcellen (zwart) of zoals voorspeld door het wiskundige model. |
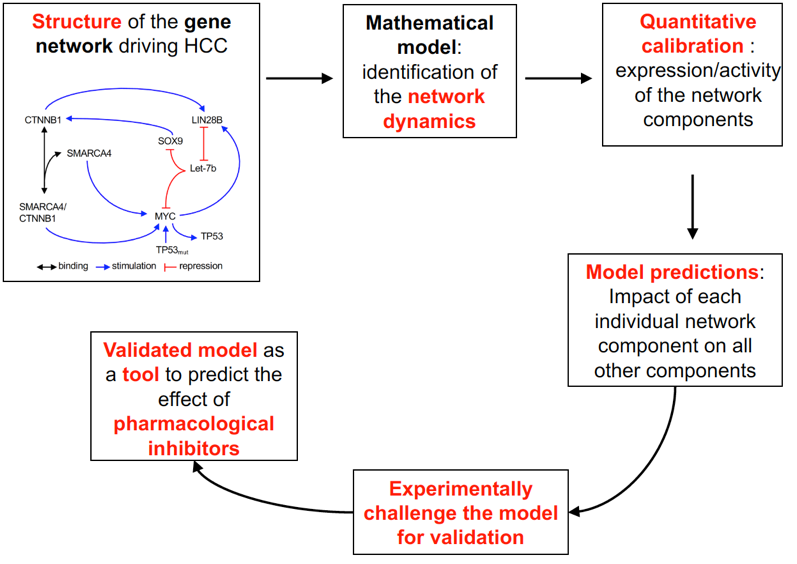
Claude Gérard, Mickael Di-Luoffo, Léolo Gonay en Frédéric Lemaigre, met hulp van de teams van Jessica Zucman-Rossi (Centre des Cordeliers, Parijs), Paul Monga (Universiteit van Pittsburgh), Emmanuel Hanert (UCLouvain, Louvain-la-Neuve) en Jens Marquardt (Johannes Gutenberg University, Mainz), ontwikkelden een wiskundig model van een gennetwerk dat een hepatocellulair carcinoom stimuleert. Het model bestaat uit een reeks vergelijkingen die de interacties van de genen in het netwerk beschrijven, en de waarden die in het model zijn geïntegreerd (expressie en/of activiteit van elke netwerkcomponent) werden experimenteel gemeten in gekweekte cellen en patiëntmonsters. Met behulp van het model voorspelden de onderzoekers hoe een therapeutisch middel gericht op één gen van het netwerk, de activiteit van alle genen die tot het netwerk behoren beïnvloedt. De methodologische stappen worden geïllustreerd in de onderstaande figuur:
 |
De aanpak helpt ook bij het karakteriseren van hoe de tumor zich ontwikkelt en draagt zo bij aan het bepalen van de prognose van de ziekte bij individuele patiënten. Het wiskundige model wordt beschikbaar gesteld aan de biomedische gemeenschap via een internet tool.
Hepatocellulaire carcinomen worden aangedreven door verschillende van dergelijke netwerken. De onderzoekers verwachten dat de identificatie en modellering van een reeks ontregelde netwerken zal bijdragen aan een globaal beeld van tumorbevorderende genfuncties bij leverkanker. De studie toont derhalve het concept van tools die helpen bij het ontwerpen van op maat gemaakte therapieën voor de behandeling van de ziekte.
Artikel over het onderzoek
Gérard C, Di-Luoffo M, Gonay L, Caruso S, Couchy G, Loriot A, Castven D, Tao J, Konobrocka K, Cordi S, Monga SP, Hanert E, Marquardt JU, Zucman-Rossi J, Lemaigre FP.
Journal of Hepatology (2019) Apr 3. pii: S0168-8278(19)30195-3. doi: 10.1016/j.jhep.2019.03.024.